Esiste una cura per la paralisi cerebrale?
È stato condotto uno studio sull’efficacia dell’infusione di cellule staminali mesenchimali del sangue del cordone ombelicale umano per i bambini affetti da paralisi cerebrale. Il CP ha attualmente due metodi di trattamento generalmente efficaci, la terapia con cellule staminali e la riabilitazione. In genere, nella terapia con cellule staminali è più conveniente utilizzare cellule umane. sangue del cordone ombelicale-MSC derivate (hUCB)-MSC), in quanto il loro uso comporta meno dilemmi etici, le cellule hanno un’immunogenicità relativamente bassa e una capacità immunosoppressiva (il che significa che è meno probabile che producano una risposta immunitaria) e hanno un tasso di proliferazione più elevato. A causa di questi benefici e potenzialità comparative, sono state condotte ricerche cliniche per studiare la sicurezza e l’efficacia dell’infusione di hUCB-MSC nei bambini con PC, e i risultati hanno dimostrato che in alcuni casi sono promettenti. Inoltre, poiché sia la terapia con cellule staminali che la riabilitazione hanno mostrato risultati positivi, il trattamento combinato è un’opzione comunemente preferita, poiché è possibile ottenere un miglioramento significativo della funzione motoria quando entrambe le terapie sono combinate. Per questo studio è stato scelto di utilizzare questo metodo combinato. Trattamento con cellule staminali per la paralisi cerebrale
Studio clinico
Lo studio è stato concepito come uno studio in singolo cieco controllato con placebo. 56 bambini sono stati arruolati nella fase di reclutamento iniziata a settembre 2010 e durata fino all’ultima visita di follow-up a settembre 2015. Solo 2 dei 56 hanno abbandonato prima del secondo corso. Tutti i pazienti sono stati assegnati in modo casuale e uniforme a due gruppi, uno con iniezioni di hUCB-MSC con riabilitazione e uno con iniezioni di soluzione salina normale (0,9% NS) con riabilitazione. Tutti i pazienti e i familiari sono stati assegnati al gruppo in cieco, ma gli sperimentatori e gli infermieri responsabili sono stati messi al corrente delle informazioni sul trattamento in modo da essere preparati a gestire eventuali emergenze, se necessario.
Le hUCB-MSC allogeniche utilizzate nello studio sono state acquisite dalla banca UCB della Beike Biotechnology Company (Shenzhen, Cina). Tutti i processi produttivi e i laboratori hanno rispettato gli standard delle buone pratiche di fabbricazione e delle buone pratiche tessutali. Le risorse provenivano dal sangue del cordone ombelicale e da tessuti di donne puerpere sane. Le donne sono state controllate e confermate negative per sifilide, HIV, virus dell’epatite B (HBV), toxoplasma, nubellavirus, citomegalo virus, herpes simplex virus e altri virus.
Ricerca sulle cellule staminali per la cura della paralisi cerebrale
La valutazione iniziale prima del trattamento tra i due gruppi ha mostrato una differenza minima sia nei punteggi della Gross Motor Function Measure (GMFM-88) sia nei punteggi della valutazione funzionale globale (CFA). Tuttavia, con il progredire del trattamento e della sperimentazione, l’efficacia è diventata molto più significativa per il gruppo infusione rispetto al gruppo placebo, come osservato al 3°, 6°, 12° e 24° mese di follow-up post-trattamento. Il punteggio GFMF-88, che valuta 5 aree funzionali (“sdraiarsi e rotolare”, “sedersi”, “strisciare e inginocchiarsi”, “stare in piedi” e “camminare, correre e saltare”), ha mostrato un’efficacia significativa nel gruppo di infusione, ma non ha mostrato alcun miglioramento sostanziale nel gruppo di controllo. La scala CFA, che valuta la cognizione, la competenza linguistica, la cura di sé, la funzione motoria e l’adattabilità sociale, ha mostrato il suo stato di efficacia 6 mesi prima della scala GMFM-88. Questo dimostra che i pazienti potevano sperimentare miglioramenti più completi prima di iniziare a mostrare miglioramenti nella funzione motoria lorda.
Un grafico delle variazioni dei punteggi GMFM-88 è riportato nella Figura 2:
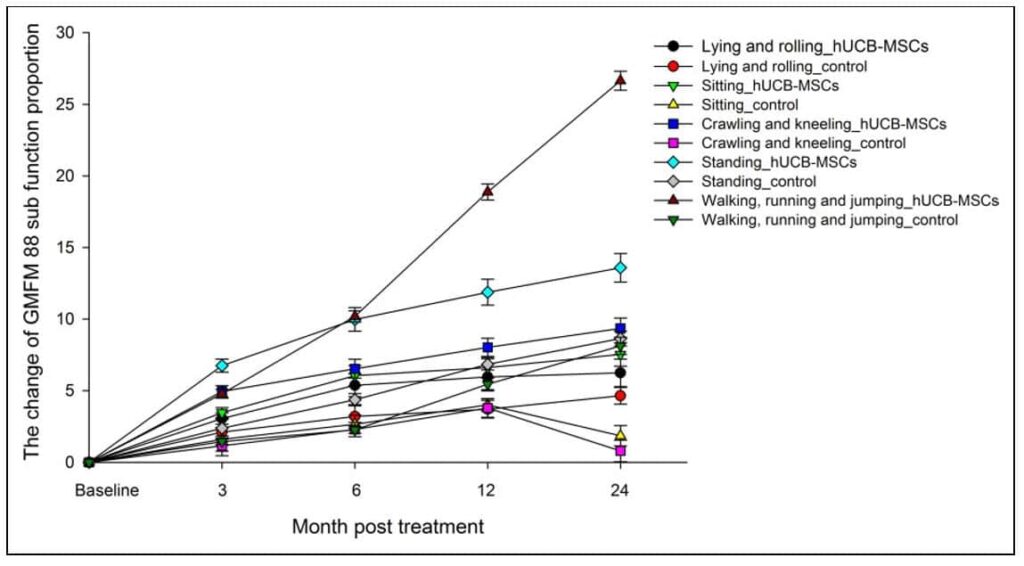
Ulteriori dati che mostrano i miglioramenti nei punteggi CFA sono riportati nella Figura 4:
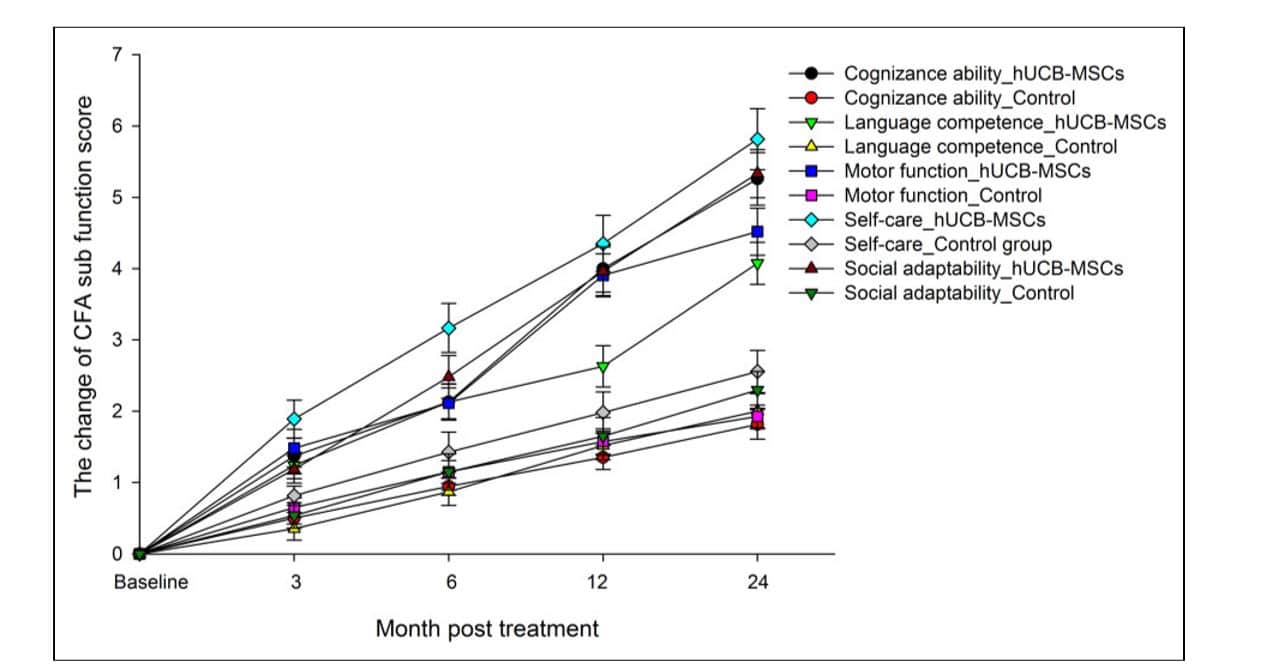
Per informazioni più approfondite sullo studio, cliccare sul link sottostante.